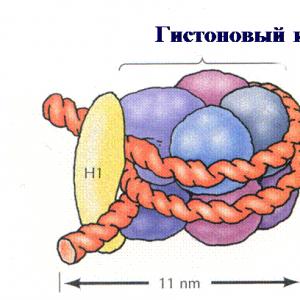
Цитомегаловирусный колит. Поражение прямой кишки и перианальной области при цитомегаловирусной инфекции
Долго я думал, необходима ли такая статья на сайте, и, проанализировав поисковые запросы от популярных поисковых систем, пришел к выводу, что людям интересна роль цитомегаловируса (ЦМВ) в жизни больных неспецифическим язвенным колитом (НЯК) и болезнью Крона (БК) . Тем более, что статья о вирусе Эпштейна-Барр (ВЭБ) уже есть в копилке полезной информации данного ресурса.
Итак, что же это за зверь “ЦМВ”, как узнать о его наличии в вашем организме и, в конце-концов, что с ним делать? На эти и другие вопросы вы найдете ответы в этой публикации.
Что такое “Цитомегаловирус (ЦМВ)”?
Цитомегаловирус (ЦМВ, от лат. Cytomegalovirus , CMV) – это вирус герпеса 5-го типа (в отличие от , который является вирусом герпеса 4-го типа). Дословно расшифровывается как “большая ядовитая клетка”, что неспроста: зараженные клетки приобретают гигантские размеры, накапливая скопления частиц возбудителя. Синтез вируса происходит в лейкоцитах и завершается образованием дочерних вирусных частиц, которые, выходя из пораженной клетки, воздействуют на рецепторы ближайших клеток и атакуют их.
Средние размеры вириона (вирусной частицы) цитомегаловируса составляют 150-200 нм (против 150 нм у ВЭБ).
Как правило, в организме здорового человека этот вирус остается незамеченным ввиду отсутствия каких бы то ни было симптомов: в ответ на возбудителя, иммунная система вырабатывает соответствующие иммуноглобулины; по статистике, антитела обнаруживают у 10-15 % подростков и 40 % людей от 30-35 лет (wikipedia).
К механизмам заражения ЦМВ относятся:
- Алиментарный (при поцелуях, рукопожатиях и т.п.).
- Контактно-бытовой (через предметы общего пользования).
- Половой.
- Трансмиссионный (через кровь).
- Вертикальный (от матери к плоду во время , во время родов, а также через молоко матери при грудном кормлении ребенка).
Следует отметить, что контактно-бытовым путем заразиться цитомегаловирусом весьма непросто. Однако, если не соблюдать элементарных правил гигиены, даже низкая контагиозность (степень “заразности”) вируса не покажется преградой.
Как и ВЭБ (да и впрочем как и любой герпесвирус), ЦМВ может бессимптомно пребывать в организме человека в течение длительного времени. Это свойство (длительное сохранение активности) называется персистентностью .
 Цитомегаловирус
Цитомегаловирус Не стоит путать между собой сам цитомегаловирус и цитомегаловирусную инфекцию (ЦМВИ) . ЦМВИ – это следствие “работы” ЦМВ. В активной стадии цитомегаловирусной инфекции в крови и органах больного обнаруживаются репликации цитомегаловируса.
Цитомегаловирусная инфекция имеет 2 фазы активности – острую и “спокойную”, причем именно “спокойная” представляет собой наибольшую опасность для здоровья человека (и снова мы видим явную параллель с вирусом Эпштейна-Барр).
Острая фаза характеризуется повышением температуры тела, слабостью, головными болями, болями в мышцах и т.д. В общем и целом, симптоматика сравнима с таковой у среднестатистического больного простудой. Через некоторое время после заражения ЦМВИ, иммунная система человека начинает вырабатывать и, либо в случае слишком агрессивной атаки вируса, либо из-за ослабленного иммунитета инфекция начинает поражать внутренние органы – вирусу, пробившему защиту организма, незачем действовать с прежним напором. Наступает так называемая “спокойная” стадия.
Под угрозой воспаления от ЦМВИ находятся такие органы как печень, поджелудочная железа, надпочечники, почки, селезенка, сосуды глазного яблока, головной мозг и наш любимый толстый кишечник . Помимо всего прочего, цитомегаловирус оказывает влияние на центральную нервную систему (ЦНС). Помимо всего прочего, цитомегаловирусная инфекция может спровоцировать развитие таких заболеваний, как бронхит и пневмония, что создаст дополнительную нагрузку на иммунитет.
ЦМВ может оказывать весьма пагубное влияние на развитие плода в утробе матери, и даже приводить к выкидышам. Цитомегаловирус также является одной из причин детского церебрального паралича (ДЦП).
Может ли ЦМВ спровоцировать НЯК или БК?
Для начала, вам следует знать, что характер поражений толстого кишечника, вызванного цитомегаловирусом, схож с таковыми при ВЗК , и это затрудняет постановку правильного диагноза. Также, зачастую при НЯК и БК цитомегаловирусная инфекция является оппортунистской , т.е. вызванной именно ослаблением иммунной системы человека.
Ранние исследования подтверждали возникновение ВЗК из-за ЦМВ, однако, позже ученые пришли к выводу, что все-таки сначала были НЯК или БК, а уже на фоне лечения основного заболевания произошла активация цитомегаловируса.
Вы же знаете, что в тяжелых случаях , таких как Азатиоприн, Метотрексат, Сандиммун и пр.? Теоретически, все латентно-инфицированные пациенты с воспалительными заболеваниями кишечника, получающие терапию цитостатиками, не позволяют противовирусным клеткам включаться в работу. Вот именно на фоне терапии такого рода препаратами ЦМВ и может активизироваться, спустя много лет бессимптомного пребывания в ваших T-лимфоцитах.
Проанализировав ряд определенных источников, я могу сделать вывод, что цитомегаловирус, скорее всего, не может вызвать появление неспецифического язвенного колита или болезни Крона, однако может значительно ухудшить состояние больного ВЗК. Ведь основное, что мы знаем о причине воспалительных заболеваний кишечника – это несомненное участие в этом процессе нашей иммунной системы (ее чрезмерной активности). Можно ли предположить, что аутоагрессия произошла на стадии первичной выработки антител против ЦМВ? Конечно, кто нам запретит:) Однако, никаких доказательств этой теории я, увы, нигде не обнаружил.
Методы диагностики и терапии ЦМВ
С помощью каких диагностических методов можно обнаружить цитомегаловирус?
- Выявление наличия вируса в биологических жидкостях организма (слюне, моче и др.) путем выявления специфических антител методом иммунофлюоресценции (метод, основанный на использовании специфичности иммунологической реакции и чувствительности флюоресцентной микроскопии).
- ПЦР (полимеразная цепная реакция).
- Бактериологический метод.
- Установление титра антител к ЦМВ.
Для лечения цитомегаловирусной инфекции предлагается использовать IgG (
При врождённой цитомегаловирусной инфекции характер поражения плода зависит от срока заражения. Острая цитомегаловирусная инфекция у матери в первые 20 недель беременности может привести к тяжёлой патологии плода, результатом которой становятся самопроизвольный выкидыш, внутриутробная гибель плода, мёртворождение, пороки, в большинстве случаев несовместимые с жизнью. При заражении цитомегаловирусом в поздние сроки беременности прогноз для жизни и нормального развития ребёнка более благоприятен. Выраженные симптомы цитомегаловирусной инфекции в первые недели жизни имеют 10-15% инфицированных цитомегаловирусом новорождённых. Для манифестной формы врождённой цитомегаловирусной инфекции характерны гепатоспленомегалия, стойкая желтуха, геморрагическая или пятнисто-папулёзная сыпь, выраженная тромбоцитопения, повышение активности АЛТ и уровня прямого билирубина в крови, повышенный гемолиз эритроцитов. Младенцы часто рождаются недоношенными, с дефицитом массы тела, признаками внутриутробной гипоксии. Характерна патология ЦНС в виде микроцефалии, реже гидроцефалии, энцефаловентрикулита, судорожного синдрома, снижения слуха. Цитомегаловирусная инфекция - основная причина врождённой глухоты. Возможны энтероколит, фиброз поджелудочной железы, интерстициальный нефрит, хронический сиалоаденит с фиброзом слюнных желёз, интерстициальная пневмония, атрофия зрительного нерва, врождённая катаракта, а также генерализованное поражение органов с развитием шока. ДВС-синдрома и смерти ребёнка. Риск летального исхода в первые 6 нед жизни новорождённых с клинически выраженной цитомегаловирусной инфекции составляет 12%. Около 90% выживших детей, страдавших манифестной цитомегаловирусной инфекции, имеют отдалённые последствия заболевания в виде снижения умственного развития, нейросенсорной глухоты или двустороннего снижения слуха, нарушения восприятия речи при сохранении слуха, судорожного синдрома, парезов, снижения зрения. При внутриутробном заражении цитомегаловирусом возможна бессимптомная форма инфекции с низкой степенью активности, когда вирус присутствует только в моче или слюне, и высокой степенью активности, если вирус определяют в крови. В 8-15% случаях антенатальная цитомегаловирусная инфекция, не проявляясь яркой клинической симптоматикой, ведёт к формированию поздних осложнений в виде ухудшения слуха. снижения зрения, судорожных расстройств, задержки физического и умственного развития. Фактором риска развития заболевания с поражением ЦНС служит стойкое наличие в цельной крови ДНК цитомегаловируса в период от момента рождения ребёнка до 3 мес жизни. Дети с врождённой цитомегаловирусной инфекции должны находиться под медицинским наблюдением в течение 3-5 лет, так как нарушение слуха может прогрессировать в первые годы жизни, а клинически значимые осложнения - сохраняться и через 5 лет после рождения.
При отсутствии отягощающих факторов интранатальная или ранняя постнатальная цитомегаловирусная инфекция протекает бессимптомно, проявляется клинически лишь в 2-10% случаях, чаще в виде пневмонии. У недоношенных ослабленных детей с низким весом при рождении, заражённых цитомегаловирусом во время родов или в первые дни жизни путём гемотрансфузий, уже к 3-5-й нед жизни развивается генерализованное заболевание, проявлениями которого служат пневмония, затяжная желтуха. гепатоспленомегалия, нефропатия. поражение кишечника, анемия, тромбоцитопения. Цитомегаловирусная инфекция носит длительный рецидивирующий характер. Максимальная летальность от цитомегаловирусной инфекции приходится на возраст 2-4 мес.
Симптомы цитомегаловирусной инфекции приобретённой у детей старшего возраста и взрослых зависит от формы инфекции (первичное заражение, реинфекция, реактивация латентного вируса), путей заражения, наличия и степени выраженности иммуносупрессии. Первичное инфицирование цитомегаловирусом иммунокомпетентных лиц обычно протекает бессимптомно и лишь в 5% случаев в виде мононуклеозоподобного синдрома, отличительными признаками которого выступают высокая лихорадка, выраженный и длительный астенический синдром, в крови - относительный лимфоцитоз. атипичные лимфоциты. Ангина и увеличение лимфатических узлов не характерны. Заражение вирусом путём гемотрансфузий или при трансплантации инфицированного органа приводит к развитию острой формы заболевания, включающего высокую лихорадку, астению, боли в горле, лимфаденопатию, миалгию. артралгию, нейтропению, тромбоцитопению, интерстициальную пневмонию, гепатит, нефрит и миокардит. При отсутствии выраженных иммунологических нарушений острая цитомегаловирусная инфекция переходит в латентную с пожизненным присутствием вируса в организме человека. Развитие лммуносупрессии ведёт к возобновлению репликации цитомегаловируса. появлению вируса в крови и возможной манифестации заболевания. Повторное попадание вируса в организм человека на фоне иммунодефицитного состояния также может быть причиной виремии и развития клинически выраженной цитомегаловирусной инфекции. При реинфекции манифестация цитомегаловирусной инфекции происходит чаще и протекает более тяжело, чем при реактивации вируса.
Для цитомегаловирусной инфекции у лммуносупрессивных лиц характерно постепенное в течение нескольких недель развитие заболевания, появляются симптомы цитомегаловирусной инфекции в виде быстрой утомляемости, слабости, потери аппетита, значительного снижения веса, длительной волнообразной лихорадки неправильного типа с подъёмами температуры тела выше 38.5 С, реже - потливости по ночам, артралгии и миалгии. Данный комплекс симптомов носит название «ЦМВ-ассоциированный синдром». У детей младшего возраста начало заболевания может протекать без выраженного начального токсикоза при нормальной или субфебрильной температуре. С цитомегаловирусной инфекцией связан широкий спектр органных поражений, одними из первых страдают лёгкие. Появляется постепенно усиливающийся сухой или малопродуктивный кашель, умеренная одышка, нарастают симптомы интоксикации. Рентгенологические признаки лёгочной патологии могут отсутствовать, но в период разгара болезни часто на фоне деформированного усиленного лёгочного рисунка определяют двусторонние мелкоочаговые и инфильтративные тени, расположенные преимущественно в средних и нижних отделах лёгких. При несвоевременной постановке диагноза возможно развитие дыхательной недостаточности, респираторного дистресс-синдромма и летальный исход. Степень поражения лёгких у больных цитомегаловирусной инфекцией варьирует от минимально выраженной интерстициальной пневмонии до распространённого фиброзируюшего бронхиолита и альвеолита с формированием двустороннего полисегментарного фиброза лёгких.
Нередко вирус поражает пищеварительный тракт. Цитомегаловирус - основной этиологический фактор язвенных дефектов пищеварительного тракта у больных ВИЧ-инфекцией. Типичными признаками цитомегаловирусного эзофагита выступают лихорадка. загрудинная боль при прохождении пищевого комка, отсутствие эффекта противогрибковой терапии, наличие неглубоких округлых язв и/или эрозий в дистальном отделе пищевода. Поражение желудка характеризуется наличием острых или подострых язв. Клиническая картина цитомегаловирусного колита или энтероколита включает диарею, стойкие абдоминальные боли, болезненность толстой кишки при пальпации, значительное снижение массы тела, выраженную слабость, повышение температуры. Колоноскопия выявляет эрозии и изъязвления слизистой оболочки кишки.
Гепатит - одна из основных клинических форм цитомегаловирусной инфекции при трансплацентарном заражении ребёнка, у реципиентов после пересадки печени, больных, инфицированных вирусом во время гемотрансфузий. Особенность поражения печени при цитомегаловирусной инфекции - частое вовлечение в патологический процесс желчных путей. Цитомегаловирусный гепатит характеризуется мягким клиническим течением, но при развитии склерозирующего холангита возникают боли в верхней части живота, тошнота, диарея, болезненность печени, повышение активности щелочной фосфатазы и ГГТТ, возможен холестаз. Поражение печени носит характер гранулематозного гепатита, в редких случаях наблюдают выраженный фиброз и даже цирроз печени. Патология поджелудочной железы у больных цитомегаловирусной инфекцией обычно протекает бессимптомно или со стёртой клинической картиной при повышении концентрации амилазы в крови. Высокой чувствительностью к цитомегаловирусу обладают клетки эпителия мелких протоков слюнных желёз, преимущественно околоушных. Специфические изменения в слюнных железах при цитомегаловирусной инфекции у детей встречаются в подавляющем большинстве случаев. Для взрослых больных цитомегаловирусной инфекцией сиалоаденит не характерен.
Цитомегаловирус - одна из причин патологии надпочечников (часто у больных ВИЧ-инфекцией) и развития вторичной надпочечниковой недостаточности, проявляющейся стойкой гипотонией, слабостью, похуданием, анорексией, нарушением работы кишечника, рядом психических отклонений, реже - гиперпигментацией кожи и слизистых. Наличие у больного ДНК цитомегаловируса в крови, а также стойкой гипотонии, астении, анорексии требует определения уровня калия, натрия и хлоридов в крови, проведения гормональных исследований для анализа функциональной активности надпочечников. Цитомегаловирусный адреналит характеризуется первоначальным поражением мозгового слоя с переходом процесса на глубокие, а в дальнейшем - и на все слои коры.
Манифестная цитомегаловирусная инфекция нередко протекает с поражением нервной системы в виде энцефаловентрикулита. миелита, полирадикулопатии, полинеиропатии нижних конечностей. Для цитомегаловмирусного энцефалита у больных ВИЧ-инфекцией характерны скудная неврологическая симптоматика (непостоянные головные боли, головокружение, горизонтальный нистагм, реже парез глазодвигательного нерва, невропатии лицевого нерва), но выраженные изменения в психическом статусе (личностные изменения, грубые нарушения памяти, снижение способности к интеллектуальной деятельности, резкое ослабление психической и двигательной активности, нарушение ориентировки в месте и времени, анозогнозии, снижение контроля за функцией тазовых органов). Мнестико-интеллектуальные изменения нередко достигают степени деменции. У детей, перенёсших цитомегаловирусный энцефалит, также выявляют замедление психического и умственного развития. Исследования спинно-мозговой жидкости показывают повышенное количество белка, отсутствие воспалительной реакции или мононуклеарный плеоцитоз. нормальное содержание глюкозы и хлоридов. Клиническая картина полинеиропатии и полирадикулопатии характеризуется болевым синдромом в дистальных отделах нижних конечностей, реже в поясничной области в сочетании с чувством онемения, парастезиеи, гиперестезией, каузалгией. гиперпатией. При полирадикулопатии возможен вялый парез нижних конечностей, сопровождающийся снижением болевой и тактильной чувствительности в дистальных отделах ног. В спинно-мозговой жидкости больных полирадикулопатией выявляют повышение содержания белка, лимфоцитарный плеоцитоз. Цитомегаловирус принадлежит ведущая роль в развитии миелита у ВИЧ-инфицированных пациентов. Поражение спинного мозга носит диффузный характер и выступает поздним проявлением цитомегаловирусной инфекции. В дебюте заболевание имеет клиническую картину полинеиропатии или полирадикулопатии. в дальнейшем. в соответствии с преимущественным уровнем поражения спинного мозга, развиваются спастическая тетраплегия или спастический парез нижних конечностей, появляются пирамидные знаки, значительное снижение всех видов чувствительности, в первую очередь в дистальных отделах ног; трофические нарушения. Все больные страдают грубыми расстройствами функции тазовых органов, в основном, по центральному типу. В спинно-мозговой жидкости определяют умеренное повышение содержания белка, лимфоцитарный плеоцитоз.
Цитомегаловирусный ретинит - самая частая причина потери зрения у больных ВИЧ-инфекцией. Данная патология описана также у реципиентов органов, детей с врождённой цитомегаловирусной инфекцией, в единичных случаях - у беременных. Больные отмечают следующие симптомы цитомегаловирусной инфекции: на плавающие точки, пятна, пелену перед взором, снижение остроты и дефекты полей зрения. При офтальмоскопии на сетчатке по периферии глазного дна выявляют очаги белого цвета с геморрагиями по ходу ретинальных сосудов. Прогрессирование процесса ведёт к формированию диффузного обширного инфильтрата с зонами ретинальной атрофии и очагами кровоизлияний по поверхности поражения. Начальная патология одного глаза через 2-4 мес приобретает двусторонний характер и в отсутствие этиотропной терапии приводит в большинстве случаев к потере зрения. У больных ВИЧ-инфекцией, имеющих в анамнезе цитомегаловирусный ретинит, на фоне ВААРТ возможно развитие увеита как проявления синдрома восстановления иммунной системы.
Сенсорноневральная глухота имеет место у 60% детей с клинически выраженной врождённой цитомегаловирусной инфекцией. Снижение слуха возможно и у взрослых ВИЧ-инфицированных лиц с манифестной цитомегаловирусной инфекцией. В основе связанных с цитомегаловирусрм дефектов слуха лежит воспалительное и ишемическое повреждение улитки и слухового нерва.
Ряд работ демонстрируют роль цитомегаловируса как этиологического фактора патологии сердца (миокардит, дилатационная кардипатия), селезёнки, лимфатических узлов. почек, костного мозга с развитием панцитопении. Интерстициальный нефрит, обусловленный цитомегаловирусной инфекцией, как правило, протекает без клинических проявлений. Возможны микропротеинурия, микрогематурия, лейкоцитурия, редко вторичный нефротический синдром и почечная недостаточность. У больных цитомегаловирусной инфекцией часто регистрируют тромбоцитопению, реже умеренную анемию, лейкопению, лимфопению и моноцитоз.
Cytomegalovirus Colitis and Subsequent New Diagnosis of Inflammatory Bowel Disease in an Immunocompetent Host: A Case Study and Literature Review
Источник: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4968430/
Дизайн исследования
Сбор данных
Статистический анализ
Интерпретация данных
Подготовка рукописи
Поиск литературы
Сбор средств
Конфликт интересов: не объявлено
Пациент: мужчина, 40
Конечный диагноз: колит ЦМВ
Симптомы: боль в животе диарея желтуха
Лекарства: —
Клиническая процедура: Гибкая сигмоидоскопия Колоноскопия
Специальность: Семейная медицина
Редкое сосуществование болезни или патологии
Инфекция желудочно-кишечным цитомегаловирусом в иммунокомпетентном хозяине является довольно редким явлением в литературе. Есть несколько сообщений об желудочно-кишечной инфекции у иммунокомпетентных, которые затем получили новый диагноз воспалительного заболевания кишечника. Предполагается, что начальная цитомегаловирусная инфекция колита вызывает начало воспалительного заболевания кишечника.
Здесь мы сообщаем о цитомегаловирусном колите и новом диагнозе воспалительного заболевания кишечника, выявленного у 40-летнего иммунокомпетентного взрослого человека, который представил симптомы желудочно-кишечного тракта и диссеминированную цитомегаловирусную инфекцию, требующую антивирусной терапии, которая успешно лечила эпизод цитомегаловирусной инфекции. Затем он продолжал иметь стойкое симптоматическое воспалительное заболевание кишечника, подтвержденное патологией.
В этой статье мы рассмотрим литературу и исследуем редкий случай колита цитомегаловируса в иммунокомпетентном хозяине и обсудим патологию, физиологию, диагностику и лечение цитомегаловирусного колита.
Желудочно-кишечный (ГИ) цитомегаловирус (ЦМВ) колит, требующий госпитализации и антивирусной терапии, является нечастым, но знакомым диагнозом. Тем не менее, колит ЦМВ у иммунокомпетентного хозяина с новым диагнозом воспалительного заболевания кишечника (IBD) является относительно редким делом. В обзоре литературы с 1960 по 2016 год содержится примерно 33 отчета о случаях заболевания. Здесь мы опишем случай колита ЦМВ на иммунокомпетентном хозяине с новым диагнозом ИБД. Это диагноз, в котором принимают участие госпиталисты, поставщики первичной медико-санитарной помощи и поставщики неотложной помощи.
40-летний мужчина, не имеющий соответствующей прошлой истории болезни, представленный ЭД с недельной историей диареи с лихорадкой до 38,7 градуса по Цельсию, ярко-красной кровью на прямую кишку, легким головокружением и головокружением в течение последних одиннадцати дней. У пациента был подобный эпизод примерно за семь месяцев до того, который разрешался спонтанно через три недели. Он отрицает недавние зарубежные поездки или контакты с больными контактами.
При поступлении его физическое обследование было доброкачественным, кроме диффузной абдоминальной нежности, легкой желтухи и крови на цифровом ректальном экзамене. Лаборатория выявила трансанинит, но отрицательный вирусный гепатит (таблица 1). Компьютерная томография брюшной полости с оральным и внутривенным контрастом показала неспецифический колит.
Он прошел гибкую сигмоидоскопию, которая показала диффузное воспаление и склепы вместе с грубой кровью. Учитывая клиническую картину, а также данные о гибкой сигмоидоскопии, подозревали CMV и образцы патологии, отправленные для тестирования. Как только они вернулись, он был начат на IV Ганцикловире.
Патологические образцы из гибкой сигмоидоскопии и колоноскопии продемонстрировали острый криптит с образованием абсцесса склепа, характерный для острого колита. Некоторые из склепов были разветвленными, а другие отсутствовали, свидетельствуя о предыдущем сражении с разрушением и регенерацией (криптографическое искажение). Это открытие характерно для идиопатического воспалительного заболевания кишечника. Более тщательное обследование ламинированной пропририи продемонстрировало наличие характерных внутриядерных («сова глаз») и внутрицитоплазматических (крошечных эозинофильных глобул) включений ЦМВ. Наличие включений ЦМВ подтверждено иммуногистохимически (рис. 1-3).
В течение следующих нескольких дней пациент начал уменьшать частоту движений кишечника, оставался афебрильным и мог переносить оральное потребление без тошноты наряду с положительной тенденцией в своих лабораториях, как видно из таблицы 1, и, таким образом, Главная. Через месяц после выписки колоноскопия для оценки патологии кишечника демонстрирует постоянный колит от прямой кишки до печеночного изгиба и нормальную появляющуюся концевую подвздошную кишку и восходящую ободочную кишку. Биопсии соответствовали воспалительным заболеваниям кишечника (рис. 4).
Цитомегаловирус — довольно распространенный вирус с прошлым воздействием, обнаруженным у 40% -100% общей популяции на серологию . CMV является членом семейства ДНК вирусов Herpesviridae, которые состоят из вируса Эпштейна Барра (EBV), вирусов простого герпеса 1-2, вирусов герпеса человека 6-8 и Varicella Zoster. При репликации вирус проливается и выводится из крови, слюны, респираторных секретов, спермы, мочи и грудного молока .
ЦМВ может вызвать активное заболевание и скрытую инфекцию. ЦМВ имеет тенденцию оставаться бездействующим и не репликативным в эндотелиальных клетках, миелоидных клетках и фибробластах . Исследования серологии показали бимодальное распределение болезни, причем пик раннего детства, вероятно, связан с вертикальной передачей от матери и горизонтальной трансмиссией с дневных улиц, а пик в молодом возрасте, вероятно, связан с сексуальным и тесным контактом и обменом физическими жидкостями, такими как слюны и спермы .
Активная ЦМВ-инфекция (первичная инфекция) часто протекает бессимптомно, но может присутствовать с инфекционным синдромом, подобным мононуклеозу, на основе вирусного генотипа . Первичная ЦМВ-инфекция часто представляет собой лихорадку, миалгию, мягкий трансанинит, цервикальную лимфаденопатию и увеличение селезенки, хотя последние два чаще встречаются в ВЭБ, чем мононуклеоз ЦМВ .
Симптоматическая активная ЦМВ-инфекция во взрослом возрасте чаще всего проявляется в иммуносупрессии (у пациентов с иммуномодулирующими препаратами, иммуномодулирующей химиотерапией, СПИДом и пациентах с трансплантацией) и часто имеет более низкий прогноз, чем инфекция в более раннем возрасте . По оценкам, 40% людей с ВИЧ / СПИДом в конечном итоге получат угрожающие жизни или глазные ЦМВ, если их количество CD4 упадет ниже 50 / мкл . Хотя редко, когда колит ЦМВ поражает иммунокомпетентные хозяева, он часто представляет собой диарею, гематоцезию, боль в животе, тенез, лихорадку, анорексию, недомогание и потерю веса .
Золотым стандартом для диагностики колита ЦМВ является гистологическое обнаружение крупных эозинофильных интрануклеазных тел включения с окружающими гало и цитомегалическими (увеличенными) клетками 2-4 × нормальных . У 37,5% пациентов нет гистологических данных . Если не обнаружено никаких находок на окраске H & E, рекомендуется иммуногистологическое окрашивание, поскольку оно более чувствительно .
Эндоскопические данные включают в себя неоднородную эритему, экссудаты, диффузно отечную слизистую оболочку с микроразрушениями и, как следствие, глубокие язвы . Сыворотка ЦМВ ДНК ПЦР имеет быстрое время обработки 6-48 часов с переменной чувствительностью в одиночку, но более 80% соответствия с результатами антигена также . Количественные исследования более чувствительны, чем качественные исследования . IgM-антитела в крови имеют чувствительность 100% и специфичность, приближающуюся к 100%, а также для активной ЦМВ-инфекции . IgM обычно становится положительным через неделю после воздействия и IgG через 3-4 недели после воздействия . Тем не менее, учитывая тот факт, что до 61% людей с ЦМВ колитом могут не иметь положительной серологии , IgM и IgG должны анализироваться вместе с клинической ситуацией.
ЦМВ-культура из крови ранее была золотым стандартом для диагностики, но, учитывая 1-3-недельное время инкубации и чувствительность не так высоко, как ПЦР, она потеряла популярность . ЦМВ-стула ДНК ПЦР может быть более чувствительной и специфичной для органа, но на данный момент нет конкретных исследований для поддержки ее использования .
Было зарегистрировано несколько сообщений о колите ЦМВ в иммунокомпетентном состоянии, и большинство знаний клинициста основано на анекдотических переживаниях. Недавно был проведен отличный метаанализ, который изучал литературу с 1983 по 2003 год и обнаружил только 28 случаев ЦМВ-колита у пациентов без иммуномодулирующих состояний . Поскольку этот метаанализ был опубликован в 2005 году, было зарегистрировано 5 случаев (при поиске с использованием ключевых слов индексации Medline) колита ЦМВ у иммунокомпетентных хозяев, большинство из которых были у пожилых людей. Самый последний случай был опубликован в 2012 году .
В метаанализе было обнаружено, что среди лиц с невосприимчивой модуляцией сопутствующих заболеваний средний возраст составлял 70,2 года, и большинство из них были женщинами, причем 55,6% случаев заразились общинами, а оставшаяся больница приобрела; 22,2% требовали колэктомии, а у группы была смертность 22,2% (выше у мужчин и в основном связана с периоперационными осложнениями от их колектомий). В группе без сопутствующих заболеваний средний возраст был моложе 37,4 лет и 100% община приобрела. Ни у кого не было colectomies, а коэффициент смертности составлял 10%. Ни один из умерших пациентов не достиг возраста 55 лет .
Серология CMV была доступна только для 38,6% пациентов, и только 13 были IgM-сыворотки. Таким образом, только IgM не является чувствительным маркером активного колита ЦМВ. Большинство случаев были ограничены левым двоеточием, что обеспечивало гибкую сигмоидоскопию или полную колоноскопию соответствующих диагностических инструментов .
Большинство пациентов в обзоре литературы были> 55 лет со средним возрастом 61,1 года. Учитывая более высокий уровень сопутствующих заболеваний в этой возрастной группе и ослабление клеточного и гуморального иммунитета, связанного с возрастом, понятно, что отсутствие смертности в возрастной группе
Хорошо известно, что у индивидуумов, уже имеющих диагноз IBD, как правило, ухудшается их заболевание, когда они инфицированы ЦМВ, приводящими к колитам, а также увеличивают заболеваемость преломляющим IBD лекарственного средства . Интересно, что среди группы
Таким образом, авторы метаанализа пришли к выводу, что колит ЦМВ полностью разрешен у лиц моложе 55 лет. В старших группах клинические переменные, такие как сопутствующие заболевания и тяжесть заболевания, определяли результат
Для многих инфекция может быть решена сама по себе, поэтому стратегия ожидания и ожидания была предложена в качестве управления первой линией в стабильном системном ЦМВ с симптоматическим управлением.
В настоящее время согласованное фармакологическое лечение системного ЦМВ представляет собой IV Ganciclovir, нуклеозидный аналог, который активируется вирусом . Он начинается при 5 мг / кг внутривенно каждые 12 часов в течение двух-трех недель и до четырех недель при тяжелой колит. Если пациенты могут переносить и принимать пероральные препараты, IV часто заменяется на ПО через пять дней . Побочные эффекты для мониторинга включают миелотоксичность, которая возникает у 40% пациентов .
Пациент, представленный здесь, был уникален тем, что он был иммунокомпетентным без предшествующих сопутствующих заболеваний или химиотерапии и был моложе среднего возраста тех похожих случаев, описанных в литературе. Вероятно, у него был субклинический IBD и начальная вспышка 7 месяцев назад. Его субклинический IBD, возможно, сделал его более восприимчивым к инфекции CMV. Обзор первоначальной патологии показывает, что, несмотря на наличие абсцессов склепа и множественных воспалительных клеток, было малочисленности тел включения, хотя и присутствующих. Если ЦМВ-инфекция дошла до ИБД, присутствие органов включения было бы более выраженным; то есть для колита ЦМВ, чтобы вызвать описанные симптомы, вирусная нагрузка, вероятно, была бы выше. Таким образом, воспаление, вероятно, было связано с IBD, с наложенной системной инфекцией ЦМВ. После того как пациент был обработан ганцикловиром, системная ЦМВ-инфекция очищалась, но пациент оставался симптоматичным от своего IBD. Его сопровождали в клинике, и, хотя его колит ЦМВ разрешался, у него продолжалось симптоматическое ИББ в течение следующих 6 месяцев.
В общем, системный колит ЦМВ чаще всего поражает иммунодефицитом. Это редко встречается в иммунокомпетентности, но следует учитывать, когда исключены более распространенные этиологии. Изолированный колит ЦМВ у иммунокомпетентного молодого пациента имеет тенденцию разрешаться с минимальными осложнениями и даже спонтанным разрешением в некоторых случаях; некоторые из них остаются с диагнозом IBD. Повышенная смертность среди пожилых людей по многочисленным причинам, включая более высокую распространенность сопутствующих заболеваний. Поэтому очень важно своевременно диагностировать колит ЦМВ, чтобы обеспечить адекватное лечение и разрешение инфекции.
Роберт Э. Джеймс, III, M.D., доктор философии, директор по патологии и лабораторной медицине, медицинский центр округа Вентура. Помощь в приобретении и интерпретации изображений патологии.
Конфликт интересов
отдел скорой помощи;
воспалительное заболевание кишечника;
желудочно-кишечный тракт;
цитомегаловирус;
иммуноглобулин, тип G;
иммуноглобулин, тип М;
иммуноферментный анализ;
иммуноферментный анализ с использованием фермента;
антитела;
гематоксилин и эозин
Средняя мощность (100 ×) H & E: Репрезентативный вид мощности среды, демонстрирующий умеренный смешанный (острый и хронический) воспалительный инфильтрат, острый криптит с образованием абсцесса склепа и криптографические искажения.
Высокая мощность (400 ×) H & E: представление высокой мощности, демонстрирующее типичные внутриядерные («глаза совы») и внутрицитоплазматические (крошечные эозинофильные глобулы) включения CMV.
Высокая мощность (400 ×) Иммуногистохимическое окрашивание для ЦМВ с контрастным пятном гематоксилина. Репрезентативный вид высокой мощности, демонстрирующий сильную фокальную CMV иммунореактивность.
Репрезентативное изображение, показывающее хронический активный колит с острым острого криптота, образование абсцесса склепа, реактивные эпителиальные изменения и фокальное мягкое криптографическое искажение, соответствующее воспалительному заболеванию кишечника (IBD).
Соответствующие лабораторные результаты.
Панель гепатита: поверхность Hep B Ag, поверхность Hep B Ab, Hep B core Ab, HepA Ab, Hep A Ig, Hep C Ab;
IBD Serology 7 Нормальные значения: ASCA IgA Elisa
IgA Elisa 14.9 (отрицательный), ASCA IgG Elisa 25,8 (отрицательный), Anti-OmpC IgA Elisa 6.0 (отрицательный), Anti CBir1 Elisa 8.2 (отрицательный), pANCA AutoAb Elisa 19.3 (положительный), IFA Перинуклеарная картина не обнаружена, чувствительность ДНК обнаружено. Подробности можно найти по адресу http://www.prometheuspatients.com/Products_Diagnostics.asp.
клинический случай
© Д. о. Маркова, М. о. Ревнова, Р.А. Насыров
ГБоУ ВПо «Санкт-Петербургский государственный педиатрический медицинский университет» минздрава россии
Резюме. Цитомегаловирусная инфекция желудочно-кишечного тракта является относительно распространенным проявлением у больных, получающих иммуносупрессивную терапию, ВИЧ-инфицированных или реципиентов органов и тканей. Однако в некоторых случаях, у иммунокомпетентных лиц также может развиваться цитомегаловирусная болезнь с поражением кишечной стенки. В особенности недавние исследования выявили потенциальную связь между ЦМВ-индуцированным колитом и различными формами воспалительных заболеваний кишечника (ВЗК). Стандартная диагностика цитомегаловирусной инфекции в биопсийном материале основана на выявлении типичных внутриядерных включений при окраске гематоксилин-эозином. Однако чувствительность данного метода для диагностики ЦМВ низкая. Иммуногистохимическое исследование биопсийного материала является чувствительным и высокоспецифичным методом. В настоящее время считается, что метод иммуногистохимии для диагностики ЦМВ является «золотым» стандартом. Некоторыми авторами сделан вывод, что наличие ЦМВ инфекции играет важную роль в усугублении течения болезни в группе больных ВЗК. Эти исследования предполагают, что у некоторых пациентов цитомегаловирусное поражение кишечной стенки может лежать в основе рефрактерного к терапии течения ВЗК.
Ключевые слова: цитомегаловирус; воспалительные заболевания кишечника; иммуногистохимический метод.
УДК: 616.34-002+616.9
цитомегаловирусная инфекция у вольных с воспалительными заболеваниями кишечника
Герпес (от греч. herpes - ползучий) - одна из наиболее распространенных и плохо контролируемых инфекций человека . Герпес-вирусы могут циркулировать в организме с нормальной иммунной системой бессимптомно, но у людей с иммуносупрессией вызывают тяжелые заболевания со смертельным исходом . По данным ВОЗ, смертность от герпетической инфекции среди вирусных заболеваний находится на втором месте (15,8 %) после гепатита (35,8 %) . На сегодняшний день открыто более 80 представителей семейства вирусов герпеса (Herpesviridae), из которых 8 типов патогенны для людей. Все 8 типов представлены ДНК-содержащими вирусами с единой морфологией, не дифференцируемой при электронной микроскопии .
Цитомегаловирус (ЦМВ) - это важный человеческий патоген, вызывающий различные синдромы, от асимптоматического течения инфекции до жизнеугрожающих органных поражений. Цитомегалови-русная инфекция желудочно-кишечного тракта является относительно распространенным проявлением у больных, получающих иммуносу-прессивную терапию, ВИЧ-инфицированных или реципиентов органов и тканей . Однако в некоторых случаях, у иммунокомпетентных лиц также может развиваться цитомегаловирусная болезнь с поражением кишечной стенки. В особенности недавние исследования выявили потенциальную связь между ЦМВ-индуцированным колитом и различными формами воспалительных заболеваний кишечника (ВЗК) .
ЦМВ представляет собой ДНК-содержащий вирус семейства Herpesviridae. При размножении ЦМВ действует цитопатически с образованием гигантских клеток с типичными внутриядерными и цито-плазматическими включениями . Так, в Великобритании и США серопозитивны 40-60 % взрослого населения среднего и высокого социально-экономического уровня (в популяции с низким социальным статусом - 80 %). В развивающихся странах распространенность ЦМВ-инфекции еще более высокая - 80 % детей и почти все взрослое население . Хотя ЦМВ - широко распространенный возбудитель и большинство людей заражаются им на каком-то этапе своей жизни, данный вирус не отличается высокой контагиозностью, и для его передачи требуется близкий или интимный контакт между людьми с инфицированными секретами (кровь, моча, слюна, сперма, цервикальное отделяемое и т. д.) . Считается, что почти в половине (43-53 %) случаев источником ЦМВ для взрослых являются инфицированные дети, которые в течение многих лет выделяют вирус с мочой и слюной . Поэтому к группе повышенного риска инфицирования относятся женщины, работающие с детьми в детских садах и других дошкольных учреждениях. В США ежегодно частота ЦМВ-инфицирования в таких группах составляет 8-20 %, тогда как в обычной популяции - 3-5 %.
КЛИНИЧЕСКИЙ СЛУЧАЙ
Другие пути передачи инфекции среди взрослых - при сексуальных контактах, переливании препаратов крови, пересадке органов и тканей .
При любом пути инфицирования размножение вируса происходит в клетках эпителиального происхождения. В результате этого при световой микроскопии в ядре появляются включения с диаметром, близким 10 мкм. Они вначале оксифильны, позднее становятся базофильными. Вокруг этих включений имеется зона просветления вещества ядра. Наряду с этим возникают более мелкие цитоплазматические включения диаметром до 3 мкм, они обычно светло-зофильные. Необходимо подчеркнуть, что этот характерный для цитомегалии гигантоклеточный метаморфоз, обозначаемый термином «совиный глаз», определяется не сразу, а через значительный срок (до 2 месяцев и более) после заболевания .
Наибольшей степени выраженности такой метаморфоз достигает на фоне иммунодефицитных состояний. В этом случае поражаются не только эпителиальные, но и многие другие клетки.
Таким образом, стандартная диагностика цито-мегаловирусной инфекции в биопсийном материале основана на выявлении типичных внутриядерных включений при окраске гематоксилин-эозином. Однако чувствительность данного метода для диагностики ЦМВ низкая. Иммуногистохимическое исследование биопсийного материала является чувствительным и высокоспецифичным методом. В настоящее время считается, что метод иммуно-гистохимии для диагностики ЦМВ является «золотым» стандартом . ЦМВИ характеризуется разнообразием клинических проявлений, однако у иммунокомпетентных индивидуумов заболевание протекает, как правило, клинически бессимптомно. В редких случаях картина напоминает инфекционный мононуклеоз, клинические проявления которого невозможно отличить от мононуклеоза, вызванного вирусом Эпштейна-Барр. Около 10 % всех случаев инфекционного мононуклеоза обусловлено ЦМВ .
Особое внимание обращено на способность ЦМВ и ВПГ повреждать клеточный иммунитет, оказывая иммуносупрессивное воздействие на организм и проявляя этим свой онкогенный потенциал . В период обострения происходит активизация вирусов. К тому же, длительная персистенция вирусов приводит к вторичному иммунодефициту, однако же и вторичный иммунодефицит способствует активации самих вирусов.
Длительная же персистенция вирусов приводит к необратимости клеточных и тканевых процессов в органах и системах с последующим апоптозом. Так, по последним данным литературы, реактивация
герпес-вирусов в ганглиях тройничного нерва и ан-тигенемия коррелирует с повышением уровня ци-токинов, в том числе ИФН^, ИЛ-6, ИЛ-10, ФНО-а, что является еще одним доказательством вовлеченности системы ИФН и каскада цитокинов в патогенез реактивации латентных герпес-вирусных инфекций (ВПГ, ЦМВ) .
Поэтому в патогенезе заболевания большое значение имеет иммунокомпетентность организма больного. Группой наибольшего риска для активации ЦМВ-инфекции являются лица с супрессией системы иммунитета. У таких больных часто наблюдается диссеминированная форма заболевания с вовлечением почти всех систем и органов .
Инфицирование ЦМВ и цитомегаловирусная болезнь должны быть четко разделены в представлении специалиста. Цитомегаловирусная болезнь включает в себя, помимо присутствия ЦМВ, такие клинические симптомы, как лихорадка, лейкопения и вовлечение органа-мишени . Поражение кишечной трубки является наиболее распространенной формой ЦМВИ с поражением гастроинте-стинальной системы. Хотя инфекция может иметь любую локализацию, эзофагит и колит являются наиболее часто наблюдаемыми синдромами .
Цитомегаловирусная инфекция желудочно-кишечного тракта является относительно распространенным проявлением у больных, получающих имму-носупрессивную терапию, ВИЧ-инфицированных или реципиентов органов и тканей.
Однако в некоторых случаях у иммунокомпе-тентных лиц также может развиваться цитомегало-вирусная болезнь с поражением кишечной стенки. В особенности недавние исследования выявили потенциальную связь между ЦМВ-индуцированным колитом и различными формами воспалительных заболеваний кишечника .
В группу ВЗК объединены два заболевания - болезнь Крона (БК) и язвенный колит (ЯК). Для этих заболеваний характерны различная распространенность патологического процесса в ЖКТ, разная глубина поражения слизистой оболочки кишки, определенные морфологические признаки, а также различное течение и прогноз. Несмотря на это, некоторые сходные особенности, такие как общность патогенетических механизмов развития этих заболеваний, и вследствие этого единые подходы к лечению, а также сходные клинические проявления позволяют объединять эти два заболевания в одну группу . Больные ВЗК должны рассматриваться как группа риска по манифестации ЦМВИ по нескольким причинам. Во-первых, они часто получают иммуносу-прессивную терапию (кортикостероиды, АЗА,
Таблица 1
Анамнестическая оценка предыдущих госпитализаций_
Дата Стул СОЭ мм/ч Фиброколоноскопия Терапия
Май 09 г к/образный, 2-3 р/д, примесь крови 47 Эрозивно-язвенный проктосигмоидит Салофальк, клизмы с гидрокортизоном
Октябрь-декабрь 10 г Стриктура кишки, язвенный проктосигмоидит Салофальк, а/б, индукционный курс биол-ой терапии
Июнь-июль 10 г Без динамики Салофальк, метрогил
Май 11 г Хроническая анальная трещина Салофальк, г/к внутрь 1 месяц
6-МП, ЦС-А или метотрексат). Более того, воспаление само по себе является предрасполагающим фактором, так как ЦМВ имеет явную тропность к пролиферирующим клеткам и грануляционной ткани .
Клинический случай Пациент А, 16 лет.
Анамнез жизни: ребенок от 1-й беременности, протекавшей с угрозой прерывания. Роды в 38 недель. Грудное вскармливание до 1 месяца, затем - смешанное. Прикормы с 3 месяцев - творог, кефир, после года - цельное молоко. Моторные навыки, нервно-психическое развитие по возрасту.
В 2003 г. перенес афтозный стоматит, отмечались высыпания на губах по типу Herpes labialis. Получал противовирусную терапию. Рецидив в 2004 и 2008 годах. С 2007 года - частые ОРВИ.
В 2004 г. (январь, ноябрь) - наблюдался инфекционистом с болями в животе, тошнотой, жидким стулом до 3 р/сут. (без примеси крови).
Летом 2008 года впервые отмечалась примесь крови в каловых массах в виде прожилок, стул кашицеобразный, 2-3 р/день.
В январе 09 года госпитализирован в хирургическое отделение с подозрением на «острый живот», с жалобами на боли в околопупочной и правой подвздошной области. В анализе крови впервые СОЭ 47 мм/ч.
Диагноз: болезнь Крона поставлен в возрасте 12 лет на основании клиниколабораторной картины и данных фиброколоноскопии. Получал противовоспалительную и гормональную терапию,
антибиотики широкого спектра действия. Проведен индукционный курс биологической терапии препаратом Инфликсимаб, по месту жительства в течение года получал только противовоспалительную терапию препаратом 5-АСК (табл. 1).
С июня 11 года наблюдается в СПбГПМА, отделение гастроэнтерологии. Поступил в тяжелом состоянии с жалобами на боли в животе, стул до 10 раз в сутки с примесью крови. Лабораторно отмечалась высокая параклиническая активность, повышение фекального кальпротектина до 875 мкг/г. Ребенку начата комплексная терапия: препаратами группы 5-АСК, иммуносупрессивная, гормональная и антибактериальная. Также начат индукционный курс биологической терапии. Фиброколоноскопия не выполнена по тяжести состояния. По ирригографии выявлен стеноз дистальных отделов толстой кишки без явлений кишечной непроходимости.
На фоне проводимой терапии стабилизировано общее состояние пациента, отмечалась положительная лабораторная динамика. Однако, через 6 месяцев от начала терапии появилась высокая гуморальная активность с повышениеи СОЭ до 48 мм/ч, усугубилась белково-калорийная недостаточность. При обследовании выявлен высокий уровень фекального кальпротектина, выполнена фиброколо-носкопия - язвенный проктосигмоидит, стриктура дистальных отделов толстой кишки, непроходимая для гастроскопа d 5 мм (табл. 2).
При иммуногистохимическом (ИГХ) исследовании биоптатов толстой кишки с использованием моноклональных антител к антигену цитоме-галовируса выявлена выраженная его экспрессия:
Таблица 2
Клинико-лабораторная динамика при обследовании в СПбГПМУ
0607.11г -25 % До 10 р/д, тенезмы, кровь 50 217 875 52 - а/б, 5-АСК, АЗА, г/к (пульс-терапия + внутрь), начало биологической терапии 5 мг/кг инфузии 1 и 2
08.11г. -16 % 1-2 р/д, оф 17 4 - 25 - г/к (снижение дозы), АЗА, 5-АСК, биологическая терапия 5 мг/кг, 3 инфузия
10.11г. -12 % 1 р/д, оф 36 АЗА, 5-АСК, биологическая терапия 5 мг/кг, инфузия 4
Таблица 2 (Продолжение)
Клинико-лабораторная динамика при обследовании в СПбГПМУ_
Дата Вес Стул СОЭ мм/ч ЦРБед/л ФК мкг/г PCDAI Фиброколоноскопия Терапия по результатам обследования
12.11г -12 % 1 Р/Д, лентовидный 48 10 30 Биологическая терапия 5 мг/кг, инфузия 5
02.12. -16 % 1 Р/Д, лентовидный 30 10 770 37,5 Язвенный проктосигмои-дит, стриктура дистальных отделов, непроходимая для гастроскопа d 5 мм Отмена 5 АСК и АЗА (нейтропения), а/б, г/к (пульс-терапия, внутрь), увеличение дозы биологического препарата до 10 мг/кг, инфузия 6
03.12. -16 % 1 Р/Д, лентовидный 18 отр 345 25 -
04.12г -15 % 1 Р/Д, лентовидный, примесь крови 30 5 778 20 - г/к внутрь, ганцикловир 10 мг/кг/сут 10 дней в/в
04.12. -15 % 1 р/д, лентовидный 30 отр 272 15 Частичное закрытие язвенных дефектов, стриктура проходима для колоноскопа Биологическая терапия 10 мг/кг, инфузия 7
антиген ЦМВ в виде темно-коричневых гранул выявлялся на клеточной оболочке, в цитоплазме, в ядрах клеток стромы и желез, а также в эндотелии микрососудов.
Учитывая наличие нейтропении в анализах крови, высокой параклинической активности, высокого уровня фекального кальпротектина, тяжелого язвенного поражения кишки с развитием рефрак-терности к проводимой терапии, что потребовало увеличения дозы биологического препарата, а также с учетом данных иммуногистохимии, состояние расценено как непрерывно рецидивирующее течение болезни Крона, осложненное цитомегалови-русной инфекцией.
Пациенту назначена противовирусная терапия препаратом Ганцикловир в дозе 10 мг/кг/сут в/в в течение 10 дней.
После курса терапии: снижение активности заболевания, фиброколоноскопия (выполнена тотально): выраженная положительная динамика в виде частичного закрытия язвенных дефектов, проходимости стриктуры кишки (табл. 2).
При проведенном повторном иммуногистохими-ческом исследовании биоптатов толстой кишки после курса противовирусной терапии выявлена значительно меньшая экспрессия цитомегаловируса. Антиген ЦМВ в виде гранул бледно-коричневого цвета выявлялся в цитоплазме единичных клеток стромы. Обращало также на себя внимание отсутствие антигена ЦМВ в клетках желез и эндотелии микрососудов.
Выписан с диагнозом:
Болезнь Крона толстой кишки, тяжелая форма, непрерывно рецидивирующее течение, осложненное стенозом дистального отдела толстой кишки. Цитомегаловирусная инфекция (колит).
Таким образом, рефрактерность к проводимой терапии при ВЗК у детей требует поиска причин отсутствия эффекта лечения, одной из которых может быть цитомегаловирусная инфекция. Выявление клинически значимой цитомегаловирусной инфекции у больных ВЗК требует рассмотрения вопроса о назначении пациенту противовирусной терапии.
ЛИТЕРАТУРА
1. Ершов Ф.И., Оспельникова Т.П. Современный арсенал антигерпетических лекарственных средств // Consilium Medicum. - 2001. - Т. 04, № 3.
2. Никонов А. П., Асцатурова О. Р. Цитомегаловирусая инфекция // Consilium Medicum (Педиатрия). - 2009, № 1.
3. Румянцев В. Г., Щиголева Н. Е. Болезнь Крона в детском возрасте // Consilium Medicum. - 2002. -Т. 04, № 6.
4. Самохин П.А. Цитомегаловирусная инфекция у детей: Клинико-морфологические аспекты. - М.: Медицина, 1987. - 159 с.
5. David A. Bobak. Gastrointestinal Infection Caused by Cytomegalovirus // Current Infectious Disease Reports. - 2003. - Vol. 5. - P. 101-107.
6. DohertyP. Immunologist. - 1995. - Vol. 3(5). -P. 231-233.
7. Dubinsky M. C. Serologic and laboratory markers in prediction of the disease course in inflammatory bowel disease // World J. Gastroenterol. - 2010. -Vol. 16(21). - P. 2604-2608.
8. Haywood L., Abernathy B. Infection // Sem Perinatol. -1998. - Vol. 22(4). - P. 260-266.
9. Herpesvirus Infections in Pregnancy //The 7th Ann. Meeting of the International Herpes Management Forum / Whitley R. J., Weber T., Pass R. Eds. - 1999. - P. 40-60.
10. Kaniel A, Lashner B. Cytomegalovirus colitis complicating inflammatory bowel disease // Am. Journal Gastroenterology. - 2006. - Vol. 101. -P. 2857-2865.
11. Karakozis S., Gongor E., Caceres M. et al. Life-threatening cytomegalovirus colitis in the immunocompetent patient: report of case and review of the literature. // Dis. Colon. Rectum. - 2001. - Vol. 44. -P. 1716-1720.
12. Klemola E., Kaariainen L. Cytomegalovirus as a possible cause of a disease resembling infections mononucleosis // BMJ. - 1965. - Vol. 2. -P. 1099-1102.
13. Maha M. Maher, Mahmoud I. Nassar. Acute Cytomegalovirus Infection Is a Risk Factor in Refractory and Complicated Inflammatory Bowel Disease. - Springer Science+Business Media, LLC. - 2008.
14. Sissons J. G. P., Carmishael A.J. Clinical aspects and management of cytomegalovirus infection // J. Infection. - 2002. - Vol. 44 - P. 78-83.
CYTOMEGALOVIRUS INFECTION IN THE PATIENTS WITH INFLAMMATORY BOWEL DISEASE
Markova D. O, Revnova M. O, Nasyrov R. A.
♦ Resume. Cytomegalovirus infection of the gastrointestinal tract is a relatively common occurrence in patients receiving immunosuppressive drugs, those infected with HIV, or those who are transplantant recepients. CMV infection may be diagnosed if typical intranuclear inclusion bodies are seen on standard hema-toxylin and eosin (H&E) stain. However, the sensitivity of H&E exam for CMV infection is low. Immunohistochemistry (IHC) exam performed on colon biopsy specimens is more sensitive than routine histologic exam and has excellent specificity. Currently IHC is considered the gold standard for detecting CMV CMV infection in patients with refractory or complicated IBD should be ruled out before aggressive immunosuppressive therapy for treatment-resistant disease to decrease morbidity and mortality.
♦ Key words: cytomegalovirus infection; immunohistochemistry; inflammatory bowel disease.
Маркова Дарья Олеговна - врач-педиатр, детский гастроэн- Markova Darya Olegovna - Paediatrician. Saint-Petersburg State
теролог. ГБОУ ВПО «Санкт-Петербургский государственный Pediatric Medical University. 2, Litovskaya St., St. Petersburg,
педиатрический медицинский университет» Минздрава России. 194100, Russia. E-mail: dashkasobk @mail.ru. 194100, Санкт-Петербург, ул. Литовская, д. 2. E-mail: dashkasobk @mail.ru.
Насыров Руслан Абдуллаевич - д. м. н., профессор, заведующий кафедрой патологической анатомии. ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России. 194100, Санкт-Петербург, ул. Литовская, д. 2. E-mail: [email protected].
Ревнова Мария Олеговна - д. м. н., профессор кафедры поликлинической педиатрии, заведующая педиатрическим отделением №4. ГБОУ ВПО «Санкт-Петербургский государственный педиатрический медицинский университет» Минздрава России. 194100, Санкт-Петербург, ул. Литовская, д. 2. E-mail: [email protected].
NasyrovRuslan Abdullayevich - MD, PhD, Professor, Head of the Department of Pathological Anatomy. Saint-Petersburg State Pediatric Medical University. 2, Litovskaya St., St. Petersburg, 194100, Russia. E-mail: [email protected].
Revnova Mariya Olegovna - MD, PhD, Professor, Head of the Clinical Department. Saint-Petersburg State Pediatric Medical University. 2, Litovskaya St., St. Petersburg, 194100, Russia. E-mail: [email protected].
Цитомегаловирус - широко распространенный ДНК- содержащий вирус. Его часто выявляют у больных с иммунодефицитом с помощью культурального или серологического методов исследования. Более чем у 90% больных со СПИДом развивается активная цитомегаловирусная инфекция (ЦМВ-инфекция), которая служит самой частой причиной диареи при отрицательных бактериальных посевах. При цитомегаловирусной инфекции могут возникать воспаление, кровотечение, изъязвление и перфорация ЖКТ. Обусловленный ЦМВ-инфекцией илеоколит - самое частое кишечное проявление . Клинически выраженный цитомегаловирусный проктит проявляется тенезмами, диареей, меленой или выделением неизмененной крови с каловыми массами, сопровождается снижением массы тела. Эндоскопически заболевание может проявляться как подслизистыми кровоизлияниями и эритематозными пятнами, так и множественными обширными глубокими язвами.
От цитомегаловирусной инфекции нужно отличать , и болезнь Крона. Биопсия слизистой оболочки позволяет подтвердить диагноз. При микроскопическом исследовании биоптата выявляют васкулит, нейтро- фильную инфильтрацию и крупные базофильные внутриклеточные включения, обусловленные ЦМВ. ЦМВ можно выявить при выращивании вирусной культуры из биоптата.
Медикаментозное лечение ЦМВ-инфекции осуществляют назначением ганцикловира или фоскарнета натрия. Ганцикловир по своему химическому строению похож на ацикловир, но в 50 раз эффективнее против цитомегаловируса. Оба препарата (ганцикловир и фоскарнет натрия) относят к виростатическим; их вводят внутривенно. Часто после отмены препарата развивается рецидив заболевания, что иногда требует пожизненного приема препарата внутрь.
Оперативное лечение выполняют при неостанавливающихся кровотечениях или перфорациях. Изменения, возникшие в результате ЦМВ-инфекции, нередко служат причиной экстренных оперативных вмешательств у больных, страдающих СПИДом. Наилучшие результаты получены после субтотальной колэктомии с выведением концевой илеостомы. Однако у чрезвычайно ослабленных больных риск выполнения подобной чрезвычайно велик, а смертность в течение 30 сут после такой операции достигает 50%.
Статью подготовил и отредактировал: врач-хирургВидео:
Полезно:
Статьи по теме:
- ВИЧ - РНК-содержащий ретровирус, поражающий Т-лимфоциты человека. ВИЧ передается через инфицированные физиологические жидкости организма и...
- Вирус простого герпеса - ДНК-содержащий вирус. Он эндемичен для населения США. Клинические проявления связаны с...
- Выбор способов лечения цитомегаловирусной инфекции у детей ограничен....