Смотреть что такое "пуриновые основания" в других словарях. Пурины в продуктах. Мочевая кислота в продуктах и подагра.
Cтраница 3
Конденсированной системой пиримидина являются пуриновые основания (гл.
В ДНК и РНК пуриновые основания аденин и гуанин связаны с цепью связью между N-9 пурина и С-1 (обозначаемым 1) пен-тозы. Пиримидиновые основания цитозин и тимин присоединяются своим атомом азота NI к С-1 пентозы. Фосфатные мостики между остатками пентозы соединяют 5 -углерод одного остатка с З - угле-родом соседнего.
Кислотный гидролиз РНК до пуриновых оснований и пиримиди-новых нуклеотидов, очень широко применявшийся в более ранних исследованиях (особенно до развития современных методов хро-мотографического анализа, см. обзоры71 16), используется для анализа нуклеотидного состава РНК и в настоящее время. Побочными процессами, протекающими в этих условиях, являются: расщепление гликозидной связи в производных дигидроурацила (см. гл.
При этом в качестве пуриновых оснований использовали пурин, аденин, 6-диметиламинопурин и 6-диметил-амино - 8-азапурин, и в этом случае даже для а о-ди-9 - пуринилгек-сана отклонение от аддитивности оптического поглощения оснований было значительно меньше в кислой среде (рН 1), чем в нейтральном или щелочном растворе.
Иными словами, количество пуриновых оснований в ДНК равно количеству пиримидиновых оснований.
Аминопроизводные пурина, называемые пуриновыми основаниями, имеют очень большое значение. Вместе с пиримидиновыми основаниями они входят в состав нуклеопротеидов (стр.
ПУРИНОВЫЕ ОСНОВАНИЯ
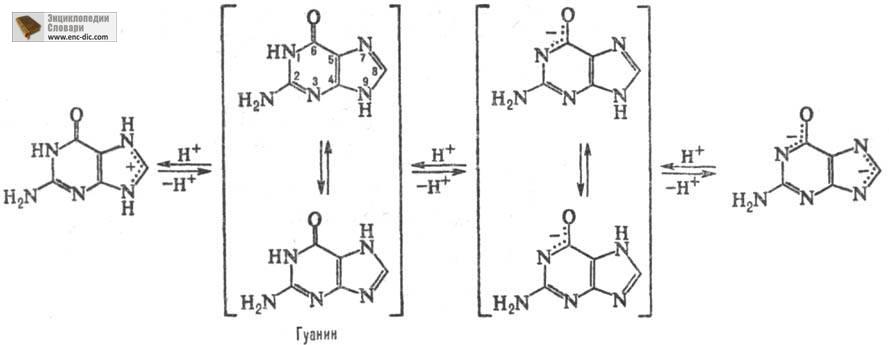
прир. производные пурина. Входят в качестве агликонов (неуглеводного компонента) в нуклеиновые к-ты, нуклеозиды, нуклеотиды; фрагменты коферментов, витаминов и др. Канонические П. о. нуклеиновых к-т-аденин (6-аминопурин, сокращенно А) и гуанин (2-амино-6-пуринон, G). Разл. формы молекул П. о., к-рые существуют при разных значениях рН, и таутомерные формы показаны на схеме: Кроме канонических П. о. в состав нуклеиновых к-т входят т. наз. минорные П. о. (см. Минорные нуклеозиды
),
гл. обр. метилированные по экзоциклич. аминогруппе и (или) по атомам N гетероцикла. Эти основания образуются фермен-тативно в составе полинуклеотидов и играют важную роль в регуляции репликации и транскрипции, в защите клеток от чужеродных ДНК (см. Рестрикция и модификация ДНК
)и системы трансляции от действия антибиотиков и др. Образование специфич. водородных связей П. о. с пирими-диновыми основаниями
в комплементарных участках цепей нуклеиновых к-т (см. Комплементарность
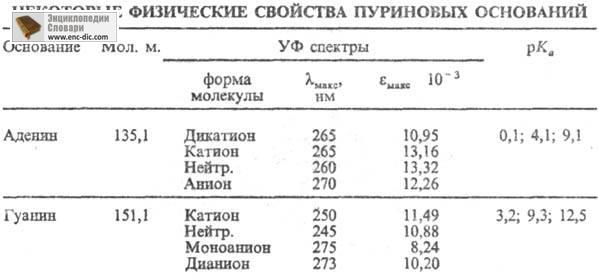
),как и межплоскостные взаимод. между соседними основаниями в поли-нуклеотидной цепи, определяют формирование вторичной и третичной структур нуклеиновых к-т. В комплементарных участках помимо канонич. пар П. о. с пиримидиновыми основаниями (А-Т и G-С; Т и С-соотв. цитозин и тимин) могут образовываться неканонич. пары (G-G, G-A, G-T и др.). Последовательность пуриновых и пиримидиновых оснований в полинуклеотидной цепи определяет генетич. информацию, заключенную в ДНК, вирусных и матричных РНК. Дезаминирование аденина в составе поли-нуклеотида (превращение в гипоксантин) меняет информац. смысл и приводит к точковой мутации. Дезаминирование гуанина (превращение его в ксантин) в составе матричных полинуклеотидов приводит к блокированию репликации и транскрипции. Метилирование П. о. по N-7 в составе матричных полинуклеотидов не сопровождается изменением генетич. смысла основания. П. о. представляют собой высокоплавкие (т. пл. > 250 °С), бесцв. кристаллич. соед., плохо раств. в горячей воде (особенно гуанин), не раств. в этаноле и диэтиловом эфире. Содержание редких таутомерных форм (иминотаутоме-ры А и G по С-6 и С-2 соотв., енольного таутомера G по С-6) не превышает в норм. условиях 10 -3 %. Протонирование и депрото-нирование П. о. сопровождается изменениями УФ спектров поглощения (см. табл.) и реакц. способности. Хорошо изучены р-ции ацилирования и дез-аминирования экзоциклич. аминогрупп П. о. действием азотистой к-ты и замещение аминогруппы аденина при действии гидроксил-аминов. Алкилирование П. о. идет по атомам N циклов (реакц. способность уменьшается в ряду: N-9 > N-7 > > N-3 > N-1), по экзоциклич. аминогруппам и по атому О-6 гуанина. Возможно прямое га-логенирование по атому С-8. При действии орг надкислот на аденин образуются N-оксиды по атомам N имида - зольного цикла. При действии формальдегида образуются N-ме-тилольные соединения. Хлор- и бромацетальдегид избирательно реагирует с аденином, образуя т. наз. этеноаденин в результате взаимод. альдегидной группы с аминогруппой аденина и последующего N-1 алкилирования с участием а-атома С реагента. Глиоксаль и кетоксаль избирательно реагируют с гуанином, образуя третий гетероцикл в результате р-ций карбонильных групп агента с экзоциклич. аминогруппой и атомом N-1. Скорости всех этих р-ций весьма существенно зависят от локальных особенностей высшей структуры полинуклеотида, что широко используют для изучения вторичной и третичной структур нуклеиновых к-т. Канонические и минорные П. о. могут быть получены препаративно из нуклеиновых к-т путем кислотного гидролиза и послед. разделения. Гуанин в больших кол-вах получают из рыбьей чешуи. Лит.
см. при ст. Муимидиновые основания. Э. И. Будовский.
На основе типичных представителей азотистых гетероциклов – пиридина и пиррола – можно рассмотреть соединения, которые содержат более одного гетероатома в молекуле.
Особенности строения оснований пиримидина и пурина:
1) это бесцветные кристаллические вещества;
2) пиримидин – шестичленный цикл, подобный пиридину, который отличается от него наличием в молекуле еще одного гетероатома (азота) вместо группы СН; 3) пурин является бициклическим.
Особый интерес представляют не столько пиримидин и пурин, сколько вещества с их характерной структурой – пиримидиновые и пуриновые основания, которые входят в состав природных высокомолекулярных веществ – нуклеиновых кислот, которые осуществляют синтез белков в организмах.
Структурные формулы пиримидиновых оснований:
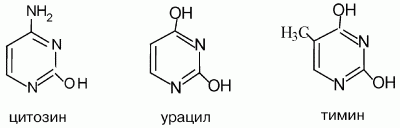
Цитозин – (2-гидрокси-4-аминопиримидин) – бесцветное малорастворимое вещество с Т пл 320–325 °C. Цитозин является слабым основанием, сравнимым с анилином и очень слабой NH-кислотой. Цитозин входит в состав нуклеиновых кислот. Урацил (2,4-дигидроксипиримидин) – бесцветное малорастворимое в воде вещество с Т пл 335 °C. Входит в состав нуклеиновых кислот, нуклеотидов. Получают из гидролизатов нуклеиновых кислот. Урацил вступает в реакции электрофильного замещения: алкилирования, галогенирования, азосочетания. Тимин (2,4-дигидрокси-5-метилпиримидин) – бесцветное малорастворимое кристаллическое вещество с Т пл 318 °C. Являясь производным урацила, обнаруживает сходные свойства, за исключением реакций S E , поскольку 5-е положение занято метильным радикалом. Входит в состав нуклеиновых кислот, нуклеотидов, является основой лекарственных препаратов. Например, азидотимидин – лекарство против СПИДа.
Структурные формулы пуриновых оснований:
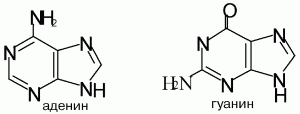
Аденин (6-аминопурин) – бесцветное кристаллическое вещество с Т пл 360–365 °C, мало растворяется в воде. Входит в состав нуклеотидов, нуклеозидов и нуклеиновых кислот. Его используют в качестве исходного соединения для органического и микробиологического синтеза и в медицине, например в качестве консерванта донорской крови. Гуанин (2-амино-6-гидроксипурин) – бесцветное кристаллическое вещество с Т пл 365 °C, мало растворяется в воде, входит в состав нуклеотидов, нуклеозидов и нуклеиновых кислот.
82. Нуклеиновые кислоты
Характерные особенности нуклеиновых кислот и теории их происхождения:
1) нуклеиновые кислоты – природные полимеры, они были обнаружены в ядрах клеток (лат. nucleus – ядро) еще в прошлом столетии, но долгое время их роль в жизни организмов была неизвестна ученым;
2) несколько десятилетий назад было расшифровано строение нуклеиновых кислот и установлено, что они играют главную роль в хранении и передаче наследственной информации и обеспечивают синтез белков в клетке.
Состав нуклеиновых кислот.
Нуклеиновые кислоты подвергаются гидролизу, при этом получается не один продукт (как у крахмала или целлюлозы), а несколько (как у белков): а) углевод (пентоза); б) азотсодержащие гетероциклические соединения (пиримидиновые и пуриновые основания); в) ортофосфорная кислота.
В организмах существуют два вида нуклеиновых кислот:
1) рибонуклеиновые (РНК);
2) дезоксирибонуклеиновые (ДНК).
Основные отличия этих нуклеиновых кислот.
1. Они различаются характером углеводного компонента – пентозы.
2. При гидролизе одних кислот образуется рибоза, в таком случае это рибонуклеиновые кислоты (РНК).
3. При гидролизе других – дезоксирибоза, это дезоксирибонуклеиновые кислоты (ДНК).
4. Различаются нуклеиновые кислоты и входящими в них азотистыми основаниями.
5. В РНК и ДНК входят по четыре основания из пяти, в их числе обязательно оба пуриновых основания – аденин и гуанин – и одно из пиримидиновых оснований – цитозин. Четвертое же основание (второе пиримидиновое) в нуклеиновых кислотах разное: в РНК это урацил, а в ДНК – тимин.
6. Неодинакова у нуклеиновых кислот и молекулярная масса: у РНК – от нескольких десятков тысяч до нескольких миллионов, ДНК – достигает даже нескольких десятков миллионов.
7. Структурными звеньями нуклеиновых кислот являются так называемые нуклеотиды.
Они выделены как промежуточные продукты гидролиза, когда процесс разложения не дошел до образования конечных продуктов.
Структурные формулы нуклеотидов.
Мононуклеотиды представляют собой фосфаты нуклеозидов, в которых фосфорная кислота связана сложноэфирной связью с одной из свободных гидроксильных групп пентозы.
Нуклеозиды – это N-гликозиды пиримидиновых или пуриновых оснований, в которых первый углеродный атом пентозы (атом углерода, обозначаемый 1) связан гликозидной связью с N-1-пиримидина или N-9-пурина.
На основе типичных представителей азотистых гетероциклов – пиридина и пиррола – можно рассмотреть соединения, которые содержат более одного гетероатома в молекуле.
Особенности строения оснований пиримидина и пурина:
1) это бесцветные кристаллические вещества;
2) пиримидин – шестичленный цикл, подобный пиридину, который отличается от него наличием в молекуле еще одного гетероатома (азота) вместо группы СН; 3) пурин является бициклическим.
Особый интерес представляют не столько пиримидин и пурин, сколько вещества с их характерной структурой – пиримидиновые и пуриновые основания, которые входят в состав природных высокомолекулярных веществ – нуклеиновых кислот, которые осуществляют синтез белков в организмах.
Структурные формулы пиримидиновых оснований:
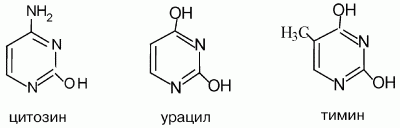
Цитозин – (2-гидрокси-4-аминопиримидин) – бесцветное малорастворимое вещество с Т пл 320–325 °C. Цитозин является слабым основанием, сравнимым с анилином и очень слабой NH-кислотой. Цитозин входит в состав нуклеиновых кислот. Урацил (2,4-дигидроксипиримидин) – бесцветное малорастворимое в воде вещество с Т пл 335 °C. Входит в состав нуклеиновых кислот, нуклеотидов. Получают из гидролизатов нуклеиновых кислот. Урацил вступает в реакции электрофильного замещения: алкилирования, галогенирования, азосочетания. Тимин (2,4-дигидрокси-5-метилпиримидин) – бесцветное малорастворимое кристаллическое вещество с Т пл 318 °C. Являясь производным урацила, обнаруживает сходные свойства, за исключением реакций S E , поскольку 5-е положение занято метильным радикалом. Входит в состав нуклеиновых кислот, нуклеотидов, является основой лекарственных препаратов. Например, азидотимидин – лекарство против СПИДа.
Структурные формулы пуриновых оснований:
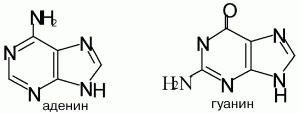
Аденин (6-аминопурин) – бесцветное кристаллическое вещество с Т пл 360–365 °C, мало растворяется в воде. Входит в состав нуклеотидов, нуклеозидов и нуклеиновых кислот. Его используют в качестве исходного соединения для органического и микробиологического синтеза и в медицине, например в качестве консерванта донорской крови. Гуанин (2-амино-6-гидроксипурин) – бесцветное кристаллическое вещество с Т пл 365 °C, мало растворяется в воде, входит в состав нуклеотидов, нуклеозидов и нуклеиновых кислот.
ПУРИНОВЫЕ ОСНОВАНИЯ ПУРИНОВЫЕ ОСНОВАНИЯ
группа природных соединений (аденин, гуанин, а также минорные П. о.); производные гетероциклич. азотистого основания пурина. Входят в состав нуклеозидов, в к-рых П. о. связаны с рибозой или дезоксирибозой, а также нуклеотидов (фосфорных эфиров нуклеозидов) - структурных компонентов нуклеиновых к-т. Содержание П. о. в ДНК равно содержанию пиримидиновых оснований; в РНК П. о. обычно больше, чем пиримидиновых. В нуклеиновых к-тах П. о. и пиримиди-иовые основания осуществляют кодирование генетич. информации и её реалит зацию в процессе биосинтеза белка. Производные П. о. играют также важную роль в биоэнергетике клетки (АТФ), в механизме гормональной регуляции (цАМФ, цГМФ), входят в состав нуклео-тидных коферментов (НАД, ФАД), витаминов, антибиотиков и др. биологически активных соединений. Биосинтез П. о. осуществляется из малых молекул (глицина, аспартата, фолиевой к-ты, СО2 и глутамина) и начинается с D-рибозо-5-фосфата, на к-ром надстраивается пури-новый цикл. В результате образуется инозиновая к-та, мононуклеотид гипоксантина - исходное соединение для синтеза аденинового нуклеотида АМФ (через стадию аденилоянтарной к-ты) и гуанинового нуклеотида ГМФ (через стадию ксантиловой к-ты). Деградация П. о., образовавшихся при распаде нуклеиновых к-т, протекает в осн. по аэробному пути по схеме: П. о. ->мочевая к-та -> аллантоин -> аллантоиновая к-та -> мочевина -> аммиак. Природа конечного азотсодержащего продукта зависит от видов животных (у большинства рыб и земноводных - мочевина, у пресмыкающихся и большинства млекопитающих - аллантоин, у приматов и нек-рых др. млекопитающих, птиц, нек-рых рептилий - мочевая к-та, у мн. беспозвоночных - аммиак, у пауков -- гуанин). У ряда организмов обнаружен анаэробный неокислит, путь распада П. о., заканчивающийся образованием глицина, муравьиной к-ты и аммиака.
.(Источник: «Биологический энциклопедический словарь.» Гл. ред. М. С. Гиляров; Редкол.: А. А. Бабаев, Г. Г. Винберг, Г. А. Заварзин и др. - 2-е изд., исправл. - М.: Сов. Энциклопедия, 1986.)
Смотреть что такое "ПУРИНОВЫЕ ОСНОВАНИЯ" в других словарях:
ПУРИНОВЫЕ ОСНОВАНИЯ - (аллоксуровые, ксантиновые), .производные пурина C5H4N4... Структурная формула пурина, установленная Э. Фишером (Fischer), представляет комбинацию пиримидинового кольца и имидазольного: При замещении в пуриновом кольце водорода у углеродного… … Большая медицинская энциклопедия
Органические природные соединения, производные пурина. К пуриновым основаниям относятся аденин, гуанин, которые входят в состав нуклеиновых кислот; продукт азотистого обмена мочевая кислота; лекарственные вещества кофеин, теобромин. Биохимическая … Википедия - производные азотистого основания пурина аденин, гуанин, ксантин и др. Биологическая роль в жизнедеятельности всех организмов обусловлена участием пуриновых оснований в построении нуклеотидов, нуклеиновых кислот, некоторых коферментов и других… … Энциклопедический словарь
Purine bases пуриновые основания. Группа химических соединений, производных пурина, входящих в виде нуклеотидов в состав нуклеиновых кислот, а также в состав коферментов
пуриновые основания - purino bazės statusas T sritis chemija apibrėžtis Adenino, guanino ir kitų gamtinių purino darinių bendras pavadinimas. atitikmenys: angl. purine bases rus. пуриновые основания ryšiai: sinonimas – purino dariniai sinonimas – purinai … Chemijos terminų aiškinamasis žodynas
Прир. производные пурина. Входят в качестве агликонов (неуглеводного компонента) в нуклеиновые к ты, нуклеозиды, нуклеотиды; фрагменты коферментов, витаминов и др. Канонические П. о. нуклеиновых к т аденин (6 аминопурин, сокращенно А) и гуанин (2 … Химическая энциклопедия
Пурины, группа природных азотистых гетероциклических соединений, производных пурина. П. о. как в свободном состоянии, так и в составе более сложных соединений играют важнейшую роль в живой природе. Так, в состав нуклеиновых кислот (См.… … Большая советская энциклопедия
Пуриновые основания - производные азотистого основания пурина (бесцветных, растворимых кристаллов аденин, гуанин, ксантин и др., участвуют в построении нуклеотидов, нуклеиновых кислот, некоторых коферментов и др. соединений. Комплементарны в ДНК к пиримидиновым… … Начала современного естествознания